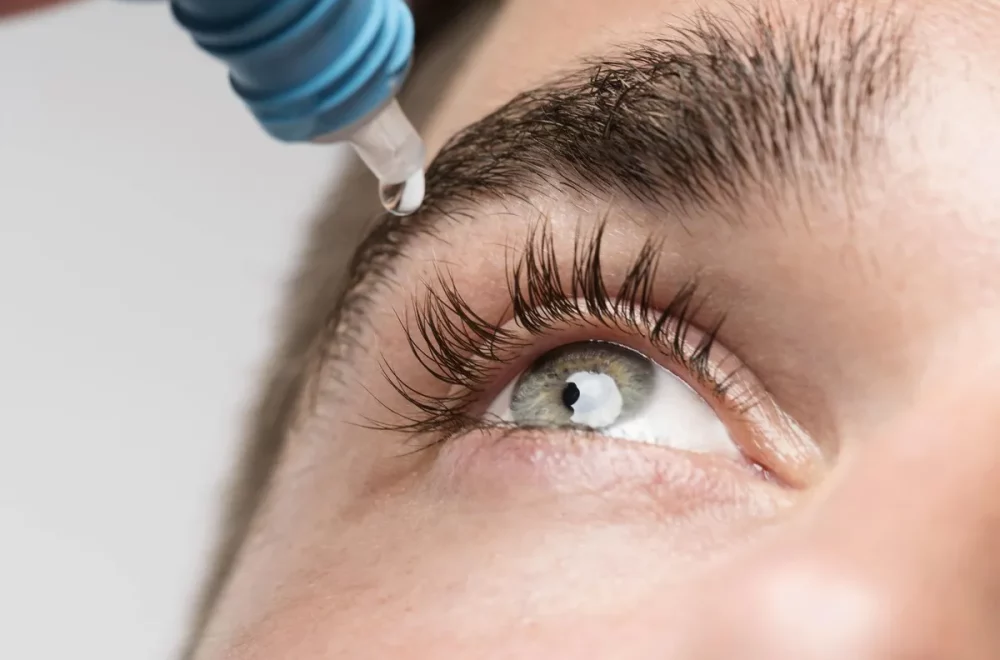
Durante el último siglo la medicina moderna ha dependido notablemente de los antibióticos. Sin embargo, la respuesta de muchos organismos ha consistido en evolucionar a súper bacterias, las cuáles son inmunes a casi cualquier medicamento.
Desde hace poco más de un año hay una en especial que ha mantenido en alerta a las autoridades de los Estados Unidos. Se trata de la Pseudomonas aeruginosa, un organismo oportunista que invade cualquier tejido comprometido.
Cuando una persona vulnerable se infecta, sus posibilidades de sobrevivir son tan solo del 50 %. Esto, debido a su resistencia a los antibióticos, por lo que puede afectar durante mucho tiempo al organismo.
Leer más: Píldora anticonceptiva de venta libre fue aprobada por la FDA
Los primeros casos de este espécimen en los Estados Unidos aparecieron en mayo de 2022 en Los Ángeles. No obstante, lo más raro de todo es que pocos días después, surgieron tres nuevos reportes. ¿A qué se debían estas infecciones?

EzriCare LLC, es unas de las marcas de gotas para los ojos retiradas del mercado
De inmediato, los Centros para el Control y la Prevención de Enfermedades (CDC) comenzaron a investigar a los infectados. Encontraron casos en Connecticut y luego en Utah. Además, descubrieron que puede contagiarse entre personas, aunque aún desconocían la fuente original.
Después de ocho largos meses de investigación descubrieron la raíz de la infección: gotas para los ojos de venta libre. Estos productos originarios de la India tenían certificación de la Administración de Alimentos y Medicamento (FDA, por sus siglas en inglés).
Las marcas con gotas infectadas eran EzriCare LLC y Delsam Pharma LLC. De inmediato, los organismos sanitarios ordenaron que se retiraran del mercado todos sus productos. ¿Cuál fue el saldo final del brote? Cuatro personas murieron, 18 más perdieron la vista y hubo otras decenas de infecciones.
En algunos casos la bacteria se expandía tan rápido que los doctores tenían que extirpar los ojos para detenerla. Mientras que en pacientes, donde no tuvo efectos tan agresivos, pasaron semanas e incluso meses antes de recuperar su visión.
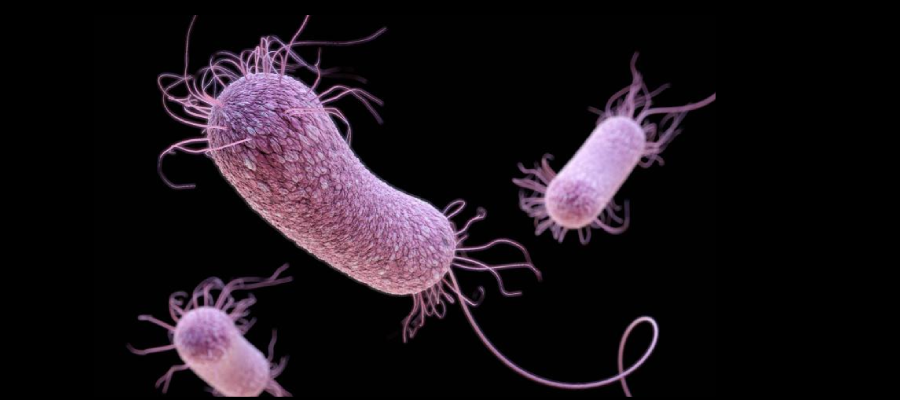
Esta supe bacteria es inmune a los antibióticos
¿Cómo estas gotas superaron los controles de la FDA?
La realidad es que los medicamentes sin recetas son de baja prioridad para la FDA. El organismo es consiente de que probablemente no funcionen, pero que lo más seguro es que tampoco causen daños mortales. En estos casos las empresas solo deben asegurar que usan los ingredientes correctos y cuentan con un procedimiento de fabricación adecuado. El resto de las restricciones que se les aplica a otros tipos de medicamentes, no aplican para estos casos.
Estas gotas no tenían garantía de esterilidad. Además, la FDA nunca inspeccionó la fábrica en dónde los hacían, por lo que no pudieron darse cuenta de esto. Lo peor del caso, es que son productos libres de conservantes. Al no tener esterilidad, ni conservantes, se convirtieron en el hogar de muchas bacterias.

Los productos Delsam Pharma LLC fueron retirados de inmediato del mercado
Jeremy Kahn, portavoz de la FDA, aseguró en un comunicado que están trabajando en mejorar los procedimientos de supervisión de productos nuevos. Asimismo, indicó que la “máxima prioridad de la agencia es proteger la salud pública”, lo que incluye mantener conversaciones con las empresas.
Según la CDC cada año mueren 35.000 personas en EE.UU por gérmenes resistentes a medicamentos. Aunque en el país, se hace seguimiento a la posible relación entre un medicamento y alguna muerte muerte, en países como la India no existe tal registro.
Desde hace años la FDA tiene retrasos para inspeccionar plantas de fabricación, sobre todo aquellas en el extranjero.
“El público estadounidense debería saber que nadie está mirando”, afirmó el profesor de la Facultad de Medicina de la Universidad de Stanford, Kevin Schulman al medio Infobae. El especialista indicó que la FDA requiere de más recursos para cumplir con sus obligaciones.
Más sobre este tema
- Masivo retiro del mercado: 5 Cheese Bread podría estar contaminado con Salmonella
- Error en etiquetado obliga a retirar del mercado cápsulas blandas de Gas-X
- Walmart retira aderezo Blackstone Parmesan Ranch por riesgo de Salmonella
- Informe sobre drones militares en Cuba desata preocupación en Florida
- ¿Comprar en outlets en EE.UU. puede costarte la visa?